经外周静脉置入中心静脉导管(peripherally inserted central venous catheter, PICC)自1995年开始在我国新生儿科应用[1],通常用于给新生儿建立长期快速的静脉通路、进行中心静脉压的监测、输入高浓度的营养液、输入对外周血管有刺激的药物、换血或部分换血。主要采取体外预估置管长度后盲穿外周静脉的方法,置管后24 h内床旁X线摄片观察定位效果。我院于2016年4月开展了床旁彩色多普勒超声引导新生儿PICC,经与以往新生儿PICC病例进行回顾性对照分析,探讨床旁彩超在新生儿PICC中应用价值,旨在减少X线对新生儿的辐射及PICC并发症。
1 材料与方法
1.1 临床资料 选取我院2016年4月至2017年6月的52例经床旁彩超引导PICC的新生儿住院病例为观察组,其中:男28例,女24例,体质量1110~3600 g,足月儿32例,早产儿20例;置管方式:右侧贵要静脉38例,右侧肘正中静脉5例,右侧腋静脉7例,右侧大隐静脉2例。选取我院2015年1—12月的42例常规行PICC的新生儿住院病例为对照组,进行回顾性分析,其中:男20例,女22例,体质量1125~3610 g,足月儿28例,早产儿14例;置管方式:右侧贵要静脉22例,左侧贵要静脉2例,右侧肘正中静脉6例,右侧颞浅静脉2例,右侧腋静脉6例,右侧大隐静脉4例。
1.2 仪器 采用迈瑞M9床旁彩色多普勒超声诊断仪,新生儿电子相控阵扇扫探头,频率1.8~2.5 MHz;线阵探头,频率7.5~10 MHz。
1.3 置管方法 两组患儿均于出生后1周内行PICC。患儿平放在红外线辐射台上,心电、呼吸、血氧饱和度监测,四肢固定,置管上腔静脉者测量穿刺点到右侧胸锁关节并向下至第3肋间的距离,置管下腔静脉者测量穿刺点到脐并向上至剑突的距离。观察组在床旁彩超线阵探头(频率7.5~10 MHz)的引导下选取粗大并走行较直的外周静脉穿刺置管,置入导管后超声全程追踪导管尖端位置,进入上腔静脉或下腔静脉后改用新生儿电子相控阵扇扫探头(频率1.8~2.5 MHz)。观察上腔静脉时探头置于患儿胸骨上窝主动脉弓切面处,探头稍向右侧偏转即可发现上腔静脉长轴,一直可追踪到与右房的连接处。观察下腔静脉采用下腔静脉长轴切面,追踪到与右房的连接处。对照组采取盲穿外周静脉的手法置管。两组新生儿置管结束后24 h内床旁X线胸腹部前后位加侧位摄片观察定位效果。
1.4 观察指标
1.4.1 PICC导管尖端最佳位置 超声定位:上腔静脉距离右房1~2 cm,下腔静脉距离右房1~2 cm[2]。X线定位:上腔静脉第3肋间,下腔静脉第8~10胸椎[3]。
1.4.2 置管成功率 置管成功率=X线摄片导管尖端到达最佳位置的例数/总例数×100%。
1.4.3 PICC的敏感度和特异度 敏感度指X线定位导管尖端位于上腔静脉或下腔静脉的最佳位置与同时超声引导PICC也定位导管尖端位于上腔静脉或下腔静脉最佳位置的概率,特异度指X线定位导管尖端不在上腔静脉或下腔静脉最佳位置与同时超声引导PICC定位导管尖端也不在上腔静脉或下腔静脉最佳
位置的概率。
1.5 统计学方法 采用SPSS 18.0统计软件分析数据。计数资料的比较采用χ2检验或Fisher确切概率法,以P<0.05为差异有统计学意义。
2 结 果
2.1 置管成功率 观察组导管尖端位于上腔静脉和下腔静脉最佳位置48例,成功率为92.31%,位于下腔静脉T11水平1例,右锁骨下静脉3例(3例均为早产儿),超声引导从右侧贵要静脉穿刺后,当导管到达右锁骨下静脉时阻力较大,尝试几次都无法再继续进管,保留置管充当外周静脉使用。对照组导管尖端到达上腔静脉和下腔静脉最佳位置30例,成功率为71.43%,导管进入右侧颈内静脉3例,折返到右侧腋静脉2例,导管进入左侧颈内静脉1例,导管尖端位置过浅位于胸锁关节水平4例,进入右房2例。观察组置管成功率显著高于对照组 (P<0.01)。见表1。
表1 两组置管成功率比较

组 别例 数成功/例失败/例成功率/%观察组5248492.311)对照组42301271.43
注:1)与对照组比较P<0.01
2.2 PICC的敏感度和特异度 观察组超声定位PICC在上腔或下腔静脉最佳位置有48例,X线摄片定位PICC在最佳位置也为48例,超声敏感度为100.00%(48/48)。X线摄片定位非最佳位置4例,超声定位非最佳位置3例,均为超声置管失败而改做外周静脉使用的病例,另1例超声定位下腔静脉最佳位置而X线摄片定位T11水平,超声特异度为75.00%(3/4)。
2.3 并发症 主要并发症为药物外渗、机械性静脉炎、导管相关性感染、导管异位和堵管。其中,观察组并发症的总发生率和药物外渗、机械性静脉炎、导管异位的发生率显著低于对照组(均P<0.05)。见表2。
表2 两组置管后并发症发生率比较
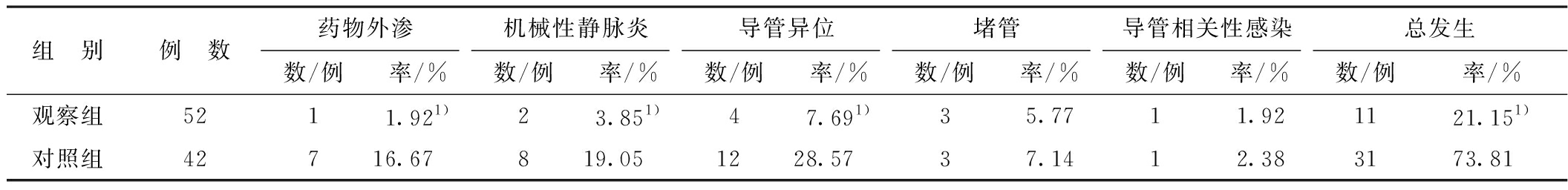
组 别例 数药物外渗机械性静脉炎导管异位堵管导管相关性感染总发生数/例率/%数/例率/%数/例率/%数/例率/%数/例率/%数/例率/%观察组5211.921)23.851)47.691)35.7711.921121.151)对照组42716.67819.051228.5737.1412.383173.81
注:1)与对照组比较P<0.05
3 讨 论
PICC穿刺置管成功的首要条件是要选取理想的外周静脉作为穿刺点。由于上肢浅静脉较下肢浅静脉短,右上肢浅静脉较左上肢浅静脉短,所以一般情况下PICC常选择右上肢肘部浅静脉作为穿刺点,主要有贵要静脉、正中静脉及头静脉。如果无法经右上肢肘部浅静脉穿刺时,也可选择腋静脉、颈外静脉或左上肢浅静脉及下肢浅静脉穿刺。新生儿外周静脉纤细,不易通过目视及触摸来选择理想的外周静脉穿刺,早产儿就更加难以通过常规的办法选取理想的外周静脉。彩色多普勒超声可显示外周血管的解剖结构及血流情况,通过彩超引导可快速准确地选择理想的外周静脉,弥补这一不足。盲穿时,由于体外导管长度测量不准确或患儿体位摆放不标准可致导管尖端位置异位到颈内静脉、锁骨下静脉、腋静脉等。以往置管后通过X线摄片定位导管尖端位置,一方面对患儿有辐射,另一方面等X线摄片结果需要一定的时间,这期间如果导管异位会对患儿造成影响。彩超引导穿刺可计算进针角度及进针深度,可全程追踪导管尖端的位置,这样就可以最大限度地避免PICC导管尖端位置过浅、过深或误入其他静脉。
导管位置过深进入右心房可引起患儿心律失常及三尖瓣损伤;过浅可引起药物外渗,其主要表现为沿导管走行的皮下软组织肿胀,由于外周浅静脉管径较上腔静脉细,药物不易稀释,可引起药物外渗。机械性静脉炎主要是选取的外周静脉管径过细、导管材质较硬、导管置入速度较快、机械性损伤静脉内膜所致。彩超可直观了解外周静脉的管径粗细,可帮助选择较粗的外周静脉作为穿刺点,减少机械性静脉炎的发生。导管堵塞主要与导管的管径粗细有关,管径越细越容易堵管。脐静脉管径较上肢肘部浅静脉粗,可选择导管的管径较PICC粗,不易堵管,早产儿1周内可选择脐静脉置管,以减少堵管的发生。导管相关性感染主要与置管前后的护理工作有关,通过加强管理及规范化操作可有效地控制导管相关性感染的发生[4]。
本研究超声引导PICC的敏感度和特异度与Michel研究的超声引导PICC敏感度和特异度分别为96.40%和93.90%[5]不同,可能与样本数量少有关。观察组中有3例导管到达右锁骨下静脉时无法继续置入,可能与早产儿右锁骨下静脉受到导管刺激后产生明显的血管痉挛有关。导管尖端位于下腔静脉T11水平的1例是由于导管置入后固定不良外加患儿活动频繁导致X线摄片时PICC导管发生向下移位所致。
综上所述,床旁彩超引导新生儿PICC准确性高,可有效减少并发症,减少X线辐射。
[1]吴旭红.新生儿PICC并发症原因分析及护理干预的研究进展[J].中国护理管理,2017,17(2):166-171.
[2]FLECTCHER S J, BODENHAM A R. Safe placement of central venous catheters:where should the tip of the catheter lie[J]. Br J Anaesth, 2000, 85(2): 188-191.
[3]邵肖梅,叶鸿瑁,丘小汕.实用新生儿学[M].4版.北京:人民卫生出版社,2011:921-922.
[4]贺望花.新生儿PICC置管机械性静脉炎的早期干预及护理对策[J].基层医学论坛,2017,21(6):642-643.
[5]MICHEL F, BREVAUT-MALATY V, PASQUALI R, et al.Comparison of ultrasound and X-ray in determining the position of umbilicalvenous catheters[J]. Esuscitation, 2012, 83(6): 705-709.