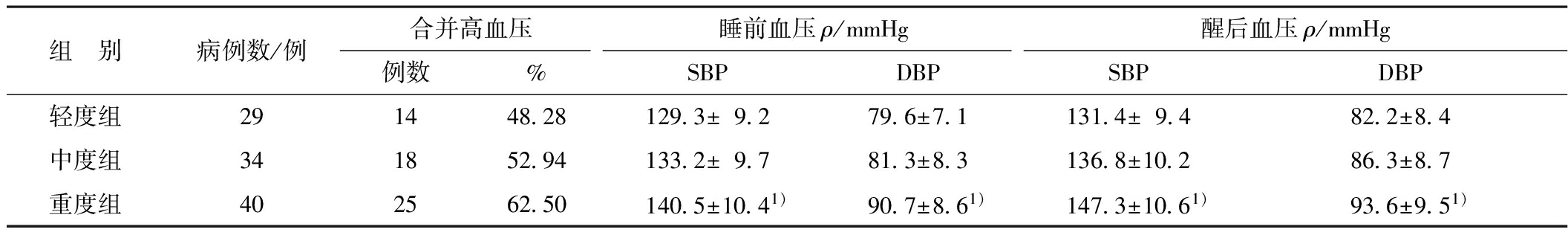
表1各组OSAHS合并高血压及监测血压情况
组 别病例数/例合并高血压睡前血压ρ/mmHg醒后血压ρ/mmHg例数%SBPDBPSBPDBP轻度组291448 28129 3±9 279 6±7 1131 4±9 482 2±8 4中度组341852 94133 2±9 781 3±8 3136 8±10 286 3±8 7重度组402562 50140 5±10 41)90 7±8 61)147 3±10 61)93 6±9 51)
张 雷
(宿迁市中医院 呼吸科,江苏 宿迁 223800)
【摘要】目的:探讨阻塞性睡眠呼吸暂停低通气综合征(OSAHS)及相关危险因素对血压的影响。方法将符合纳入标准的103例患者按呼吸暂停低通气指数(AHI)作为OSAHS病情分度标准分为轻度组29例,中度组34例,重度组40例,通过问卷调查掌握患者一般资料,入院当晚21:30采用PSG多导睡眠监测仪进行连续监测7 h以上,并与PSG监测前进行2次右臂肱动脉血压测量,并于次日晨用同样的方法测量醒后血压,通过单因素分析选择与OSAHS合并高血压相关的危险因素进行Logistic多因素回归分析。结果103例OSAHS患者中,合并高血压57例(55.34%),重度组睡前、醒后收缩压(SBP)和舒张压(DBP)明显高于轻度组和中度组(均P<0.05),OSAHS伴高血压组AHI、呼吸紊乱指数(RDI)均高于无高血压组,而最低血氧饱和度(Min SpO2)明显低于无高血压组(P<0.05),OSAHS伴高血压组在年龄、BMI值、腹围、吸烟率、总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-C)方面均明显高于无高血压组(均P<0.05),高密度脂蛋白胆固醇(HDL-C)明显偏低 (P<0.05),Logistic多元回归分析显示年龄、BMI、 TC、AHI、Min SpO2为OSAHS合并高血压的危险因素。结论OSAHS患者发生高血压的危险性与病情严重程度呈显著相关性,BMI、TC、AHI、Min SpO2为OSAHS合并高血压的危险因素。
【关键词】阻塞性睡眠呼吸暂停低通气综合征(OSAHS);高血压;危险因素;相关性
阻塞性睡眠呼吸暂停低通气综合征(obstructive sleep apnea-hypopnea syndrome,OSAHS)为睡眠呼吸暂停综合征(sleep apnea syndrome,SAS)最常见的类型,是多种原因导致睡眠状态下反复发生完全或部分上气道阻塞,引起间歇性低氧血症伴高碳酸血症及睡眠结构紊乱,进而使机体发生一系列病理生理改变的临床综合征。其主要临床表现为睡眠片段化,睡眠打鼾伴呼吸暂停,日间过度嗜睡、疲乏等,随着病情的发展可导致高血压、冠心病、心律失常、脑血管意外、糖与脂类代谢紊乱,甚至发生肺动脉高压等一系列并发症[1]。国内外研究证实OSAHS是导致高血压的独立危险因素,而高血压是OSAHS主要并发症,两者存在密切相关性,流行病学调查显示,约≥50%的OSAHS患者伴有高血压,至少30%的高血压患者并发OSAHS[2]。本研究旨在探讨OSAHS严重程度及相关因素对血压的影响。
1.1 一般资料 选择2014年1月至2015年10月于我院呼吸科就诊的OSAHS患者103例,纳入标准均符合中华医学会呼吸病学分会有关OSAHS诊治指南(2011年修订版)[3],并经临床多导睡眠图监测(polysomnography,PSG)确诊。其中:男82例,女21例;年龄42~78岁,平均(58.6±7.6)岁。排除严重心脏疾病、脑卒中、慢性阻塞性肺疾病(COPD)、支气管哮喘、糖尿病等疾病及严重肝肾功能不全患者。
高血压诊断标准参照《中国高血压防治指南(2010年修订版)》,即在未使用降压药物的情况下,非同日3次测量血压,收缩压(SBP)≥140 mmHg和(或)舒张压(DBP)≥90 mmHg。SBP≥140 mmHg和DBP≥90 mmHg为单纯性收缩期高血压。患者既往有高血压史,目前正在使用降压药物,血压虽然低于140/90 mmHg,也诊断为高血压。以呼吸暂停低通气指数(apnea hypopnea index,AHI)作为OSAHS病情分度标准[3]。将103例患者分为轻度组29例(AHI≤15次/h),中度组34例(AHI>15~30次/h),重度组40例(AHI>30次/h)。
1.2 方法 对符合纳入标准的103例患者均给予体格检查及OSAHS病情评估问卷调查,包括年龄、性别、体质量、身高、颈围、腹围、吸烟、饮酒史等,患者入院次日晨空腹抽取静脉血,检测血脂4项即总胆固醇(TC)、三酰甘油(TG)、高密脂蛋白胆固醇(HDL-C)、低密脂蛋白胆固醇(LDL-C)及空腹血糖(FBG)等指标,并根据身高、体质量计算体质量指数(body mass index,BMI),BMI值18.5~24为正常, 24~28为超重,≥28为肥胖。入院当晚21:30采用德国SOMNO screen PSG多导睡眠监测仪连续监测 7 h以上,在PSG监测前进行血压测量(测量前患者需安静休息不少于10 min),测量2次右臂肱动脉血压,并于次日晨用同样的方法测量醒后血压。行PSG监测当日嘱患者禁止饮酒、咖啡,禁用安眠药等镇静剂。监测期间注意观察记录呼吸紊乱指数(respiratory disturbance index,RDI)即睡眠中每小时阻塞性呼吸事件(包括呼吸暂停、低通气及呼吸相关性微觉醒)的次数,轻度5~15次/h,中度>15~30次/h,重度>30次/h;最低血氧饱和度(Min SpO2)(轻度>85%~90%,中度80%~85%,重度<80%)。
1.3 统计学方法 采用SPSS17.0统计软件进行数据处理,计量资料比较采用t检验,多组间比较采用方差分析(ANOVA);计数资料比较采用χ2检验,以Logistic进行多元回归分析。
2.1 各组OSAHS合并高血压及监测血压情况 结果详见表1。
表1各组OSAHS合并高血压及监测血压情况

注:1)与轻度组、中度组比较P<0.05
在103例OSAHS患者中,57例合并高血压,其中重度组睡前、醒后的SBP和DBP显著性高于轻度组和中度组。伴高血压组57例患者中,男44例,女13例。无高血压组46例患者中,男35例,女11例。
2.2 OSAHS伴高血压组与无高血压组主要睡眠呼吸参数 结果详见表2。
表2 OSAHS伴高血压组与无高血压组的主要睡眠呼吸参数

注:1)与无高血压组比较P<0.05
OSAHS伴高血压组AHI、RDI均高于OSAHS无高血压组,而Min SpO2低于无高血压组(均P<0.05)。
2.3 OSAHS伴高血压相关因素的比较 结果详见表3。
表3 OSAHS伴高血压相关因素的比较


注:1)与无高血压组比较P<0.05
与OSAHS无高血压组比较,伴高血压组年龄、吸烟率、BMI值、腰围、TC、TG、LDL-C均明显偏高,HDL-C明显偏低(均P<0.05)。
2.4 OSAHS伴高血压回归分析 以OSAHS患者发生高血压作为因变量,将未合并高血压设定为“0”,合并高血压设定为“1”;将单因素分析显示有统计学意义的自变量即年龄、吸烟率、BMI、腰围、TC、TG、HDL-C、LDL-C、AHI及Min SpO2进行多因素Logistic回归分析,其中年龄、吸烟率、腰围、TG、HDL-C、LDL-C被模型排除,而BMI、TC、AHI和Min SpO2显示为OSAHS合并高血压发病的危险因素。
OSAHS与高血压密切相关,是独立于年龄、性别、肥胖、吸烟、饮酒、精神紧张以及心脏、肾脏等疾病以外导致高血压发生和发展的危险因素,同时亦是继发性难治性高血压的危险因素之一[4]。其患者合并发生高血压的比率很高,发病机理相关因素较为复杂,研究证实可能与以下因素有关[5]。(1)微觉醒和睡眠结构紊乱:患者反复觉醒和微觉醒次数明显增多,导致其睡眠结构紊乱、睡眠质量下降和睡眠剥夺致低氧血症和高碳酸血症,刺激交感-肾上腺髓质系统兴奋,使血浆儿茶酚胺浓度增高,长此以往引起高血压发生。(2)交感神经张力:交感神经活性亢进是原发性高血压形成和维持过程中重要发病机理之一。曾利等[6]研究认为OSAHS患者反复睡眠呼吸暂停使大脑皮质下神经中枢功能紊乱,交感神经和副交感神经之间的平衡失调,交感神经兴奋性增加,其末梢释放儿茶酚胺增多,从而引起小动脉和静脉收缩,心肌收缩力加强,心率加快,心搏出量增加,导致夜间睡眠及晨起血压升高。(3)肾素-血管紧张素-醛固酮系统(RAAS)亢进: 肾素主要由肾小球旁细胞合成和分泌,可激活肝脏产生的血管紧张素原而生成血管紧张素Ⅰ(AT-Ⅰ),在血管紧张素转换酶(ACE)的作用下,转变为血管紧张素Ⅱ(AT-Ⅱ),AT-Ⅱ可激活平滑肌受体,刺激血管收缩以及促进交感神经末梢释放儿茶酚胺,并促进肾上腺皮质球状带分泌醛固酮增加血容量,收缩血管,使血压升高。朱利清等[7]通过对OSAHS及合并高血压患者血浆中AT-Ⅱ水平临床研究结果显示,OSAHS血压正常及合并高血压患者血浆中AT-Ⅱ水平较正常对照组均明显升高,说明OSAHS患者存在RAAS亢进现象,给予OSAHS合并高血压患者ACE抑制剂治疗,降血压的同时也改善睡眠呼吸障碍,表明RAAS以及AT-Ⅱ在OSAHS发生高血压中起着重要作用。(4)细胞黏附分子活性增强:OSAHS引起的间歇性低氧血症通过增强循环系统中炎症介质的活性,刺激心血管系统的炎症,尤其是动脉粥样硬化(AS)的发生,进一步对心血管疾病的发病起到促进作用。其中细胞间黏附分子-1(ICAM-1)和血管细胞黏附分子-1(VCAM-1)是OSAHS引起的低氧血症刺激下血管内皮细胞受到损伤所产生的主要炎症介质。李延忠等[8]研究发现OSAHS及合并高血压患者血清ICAM-1及VCAM-1水平明显高于正常对照组,且ICAM-1水平与AHI及微觉醒指数呈明显的正相关,与Min SpO2呈明显的负相关,表明血清ICAM-1、VCAM-1水平的升高是OSAHS患者高血压发病的重要危险因子之一。(5)血管内皮功能障碍:OSAHS间歇低氧血症(IH)/再氧合(ROX)导致氧自由基和NE和AT-Ⅱ等血管炎性物质活性增加,损害血管内皮及其功能,使得由血管内皮细胞合成和分泌对血管舒缩功能及血流动力学起重要的调节作用的ET-1和NO间相互制约、平衡关系丧失,NO水平下降,ET-1分泌增加,导致患者血管收缩、血管平滑肌增殖、管腔狭窄和血管重塑,从而促进高血压及AS的发生、发展[9]。
本研究结果显示,以AHI分组,其中重度组(AHI>30次/h)醒后SBP明显高于轻度组、中度组,提示OSAHS患者发生高血压的危险性与AHI严重程度呈显著相关性,AHI为发生高血压的危险因素。OSAHS伴高血压组AHI、RDI均高于无高血压组,而Min SpO2明显低于无高血压组,且伴高血压组在年龄、BMI值、腰围、吸烟率、TC、TG、LDL-C方面均明显偏高,而HDL-C明显偏低,多因素Logistic回归分析,发现BMI、TC、 AHI、Min SpO2为OSAHS合并高血压发病的危险因素,与国内文献报道基本一致[10-11]。表明低氧致间歇性低氧血症与OSAHS合并高血压发病呈线性相关,OSAHS可以导致血脂代谢紊乱。
综上所述,OSAHS患者发生高血压的危险性与病情严重程度呈显著相关性,BMI、TC、AHI、Min SpO2为OSAHS患者合并高血压的危险因素。因此,应加强患者的高血压预防和治疗,控制相关危险因素,以降低合并高血压的发病率。
参考文献:
[1]葛均波,徐永.内科学[M].8版.北京:人民卫生出版社,2013:128-132.
[2]乌晶,张朝军.阻塞性睡眠呼吸暂停低通气综合征与高血压病[J].内蒙古医学杂志,2012,44(1):25-28.
[3]中华医学会呼吸病学分会睡眠呼吸障碍学组.阻塞性睡眠呼吸暂停低通气综合征诊治指南(2011年修订版)[J].中华结核和呼吸杂志,2012,35(1):9-12.
[4]王海玲,王宇.阻塞性睡眠呼吸暂停低通气综合征与高血压的关系[J].中华高血压杂志,2011,19(3):227-230.
[5]张倩,张丙芳.阻塞性睡眠呼吸暂停低通气综合征与高血压的相关分析[J].心脏杂志,2015,27(4):486-489.
[6]曾利,史忠,邓国兰,等.阻塞性睡眠呼吸暂停低通气综合征对原发性高血压患者心率变异和血压节律的影响[J].中华高血压杂志,2010,18(2):124-128.
[7]朱利清,张厚德,涂向东,等.OSAHS及合并高血压患者血浆中AT-Ⅱ和ET1的临床研究[J].中华全科医学,2011,9(5):686-688.
[8]李延忠,张万荣,王廷础,等.黏附分子在阻塞性睡眠呼吸暂停低通气综合征合并高血压发病中的作用[J].中华结核和呼吸杂志,2004,27(8):511-514.
[9]詹冰洁.血管内皮功能障碍在OSAHS并发高血压发病机制中的作用[J].心脑血管病防治,2013,13(6):478-480, 486.
[10]朱小川,储德节,洪燕,等.阻塞性睡眠呼吸暂停低通气综合征与高血压的相关性及危险因素分析[J].中国临床医学,2015,22(6):750-753.
[11]黄瑞强.阻塞性睡眠呼吸暂停低通气综合征与高血压关系的前瞻性研究[D].福州:福建医科大学,2011.
【中图分类号】R563
【文献标识码】A
DOI:10.11851/j.issn.1673-1557.2017.05.019
优先数字出版地址:http://kns.cnki.net/kcms/detail/51.1688.R.20170914.1646.036.html
(收稿日期:2017-01-04)
E-mail:sqzhangleiok@126.com